Takeda
En savoir plus...
TAK341, un anticorps alpha-synucléine testé dans l’AMS
L’essai va commencer dans 3 sites français

Aux USA, en Asie et en Europe, 59 sites investigateurs, dont 3 en France, participent à l’essai clinique de phase 2 de TAK341, une immunisation passive mise au point par Takeda avec AstraZeneca.
TAK341 apporte à l’organisme des anticorps qui visent à éliminer les agrégats pathologiques d'alpha-synucléine existants mais aussi à empêcher leur formation et leur propagation. Il a déjà fait l’objet d’un essai de phase 1 mené aux USA avec 36 personnes souffrant de la maladie de Parkinson. Pour l’essai de phase 2 qui commence, c’est l’atrophie multi-systématisée que vise Takeda, avec la participation annoncée d’un total de 138 patients AMS de par le monde.
En France, 3 sites investigateurs participent à l'essai, le Centre de référence de l’AMS de Toulouse et les Centres de compétences de Marseille et Strasbourg qui assureront chacun le recrutement et le suivi d’un très petit nombre de patients-volontaires, 2 ou 3 par site tout au plus. Le Centre de référence de Bordeaux aurait souhaité s’impliquer. Il en a été empêché faute de pouvoir s’assurer la participation d’un service d’ophtalmologie pour la surveillance très étroite des patients qui s’impose dans cet essai.
Les patients-volontaires recevront 13 injections intraveineuses au cours des 52 semaines que durera cet essai en double aveugle contre placebo. L’objectif est d’évaluer les effets de l’anticorps mesurés d’après l'échelle unifiée d'évaluation de l'atrophie multi-systématisée, partie 1 (UMSARS). Deux cohortes de patients seront constituées afin d’évaluer les effets de 2 dosages de TAK341.
Les modalités d’action de l’anticorps passif TAK341 sont comparables à celles du candidat-médicament de Lundbeck ci-dessous
Mécanismes présumés de l’immunothérapie
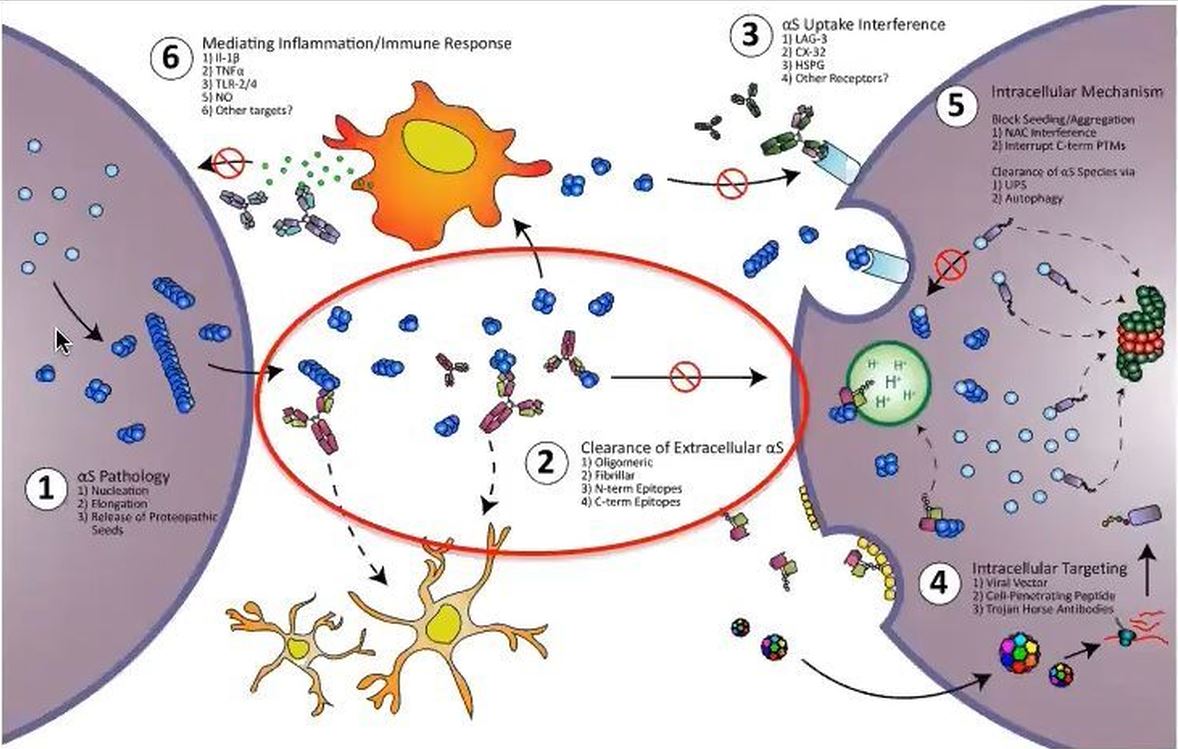
Cette image montre deux grandes cellules coloriées en gris. Dans celle de gauche on voit, en bleu, des protéines d’alpha-synucléine mal repliées. Elles sont isolées ou anormalement agglomérées en agrégats de tailles différentes. Plus ces agrégats sont gros, plus la cellule a du mal à les éliminer. Ces agrégats peuvent sortir de la cellule envahie, dans l’espace extra-cellulaire (en blanc). Ils peuvent alors être captés par l’autre cellule du cerveau, à droite, dans laquelle ils provoqueront le même processus d’agrégation et les mêmes dégâts. C’est ainsi que le mécanisme de formation de ces agrégats toxiques d’alpha-synucléine se propage, au fil de de l’évolution de la maladie.
L'immunothérapie vise à empêcher cette diffusion de la protéine alpha-synucléine déviante d’une cellule à l’autre. Elle aide le système immunitaire constitué par les cellules gliales de la microglie (en jaune, dans l’espace blanc entre les cellules), à repérer et éliminer l’alpha-synucléine toxique.
mise à jour : septembre 2023
Glossaire
Alpha-synucléine
Les dysfonctionnements de l’alpha-synucléine sont à l’origine de plusieurs pathologies appelées « synucléinopathies » : l’AMS, la maladie de Parkinson, la maladie à corps de Lewy.
L’alpha-synucléine est une petite protéine abondante dans le cerveau et nécessaire à son 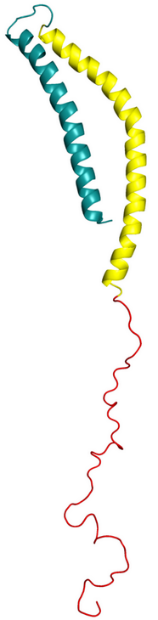 fonctionnement.
fonctionnement.
Pour des raisons inconnues, cette protéine peut adopter une mauvaise conformation, jusqu’à former des agrégats. Ces agrégats vont encombrer les neurones, mais aussi, dans l’AMS, les oligodendrocytes, ces cellules de soutien des neurones. De plus, l’alpha-synucléine mal repliée propage de cellule en cellule son fonctionnement anormal. C’est pourquoi cette protéiné encore mal connue, ses différentes souches, son mode de propagation sont la principale cible des stratégies thérapeutiques visant l’AMS et les maladies voisines.
En savoir plus :
Voir la page "Au commencemen de la recherche, les cellules oligodendriales"
Voir la vidéo « l’alpha-synucléine dans l’AMS », par Pierre-Olivier Fernagut, coordonnateur du Conseil scientifique d’Aramise.
Cellules gliales
Ce sont les cellules qui forment l’environnement des neurones. Elles jouent un rôle de soutien et de protection du tissu. Elles entourent les neurones et participent au contrôle de l'en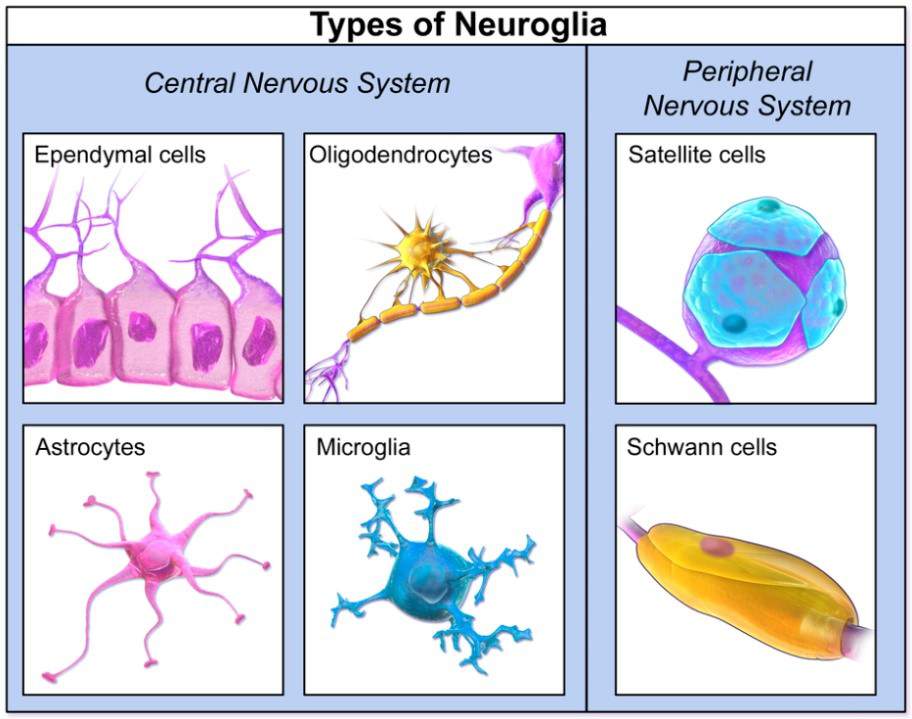 vironnement chimique et électrique en leur fournissant des nutriments, de l’oxygène et en éliminant leurs déchets. Ces cellules produisent par exemple la myéline, une substance qui sert d'isolant aux fibres nerveuses.
vironnement chimique et électrique en leur fournissant des nutriments, de l’oxygène et en éliminant leurs déchets. Ces cellules produisent par exemple la myéline, une substance qui sert d'isolant aux fibres nerveuses.
Il y aurait, dans notre système nerveux, à peu près autant de cellules gliales que de neurones, soit environ 100 milliards. Les cellules gliales sont différentes au sein du système nerveux central et du système nerveux périphérique, elles n’ont pas non plus la même origine dans leur développement.
● Les cellules gliales du système nerveux central (SNC) qui dérivent des glioblastes du tube neuronal embryonnaire, sont de 3 types :
- les astrocytes qui assurent un lien fonctionnel entre vaisseaux et neurones, apportant substrats énergétiques aux neurones et les débarrassant des produits de dégradation ;
- les oligodendrocytes à l’origine de la gaine de myéline des neurones ;
- les épendymocytes qui forment les parois qui délimitent les différentes cavités du SNC et sont responsables de la synthèse du liquide céphalo-rachidien (LCR)
● Les cellules gliales du système nerveux périphérique (SNP), dérivent des crêtes neurales embryonnaires. Ce sont les cellules satellites avec une fonction analogue à celle des astrocytes et les cellules de Schwann qui forment chacune la gaine d’un seul neurone, à la différence des oligodendrocytes qui « s’occupent » chacun d’une dizaine de neurones.
Immunothérapie
L’immunothérapie dans les synucléinopathies.
A) Pour des raisons encore mal élucidées, génétiques ou environnementales, un mauvais repliement de l’α-synucléine (en blanc l’α-synucléine normale, en jaune l’α-synucléine mal conformée) survient en intracellulaire et conduit à la formation d’agrégats oligomèriques (*) puis de fibrilles (**). Les agrégats peuvent être ensuite relargués en extracellulaire.
B) Les agrégats d’α-synucléine peuvent alors pénétrer dans de nouvelles cellules nerveuses, déclencher le mauvais repliement de l’α-synucléine normale de la cellule et provoquer la formation d’agrégats.
1) Via leur portion Fab (fragment antigen binding), les anticorps peuvent fixer les formes anormales d’α-synucléine afin de les neutraliser et/ou de favoriser leur dégradation.
2) Via leur portion Fc (fragment cristallisable), les anticorps peuvent se lier à des récepteurs situés à la surface des neurones et favoriser ainsi l‘élimination intracellulaire de l’α-synucléine, en particulier au niveau des lysosomes.
3) Les anticorps peuvent aussi se lier par leur portion Fab aux récepteurs qui permettent l’absorption des agrégats d’α-synucléine et ainsi empêcher leur internalisation.
4) Des intracorps peuvent être administrés via un plasmide et agir en intracellulaire où ils favorisent la dégradation des agrégats et/ou empêchent l’agrégation des monomères.
5) Les complexes anticorps–agrégats d’α-synucléine peuvent aussi se lier à des récepteurs présents à la surface de la microglie et déclencher leur phagocytose.
L’immunothérapie active, ou vaccination, consiste à administrer un antigène (ici l’α-synucléine anormale ou des fragments d’α-synucléine anormale), pour déclencher une production d’anticorps spécifique, par le système immunitaire (réponse humorale).
L’immunothérapie passive consiste en l’administration directe d’anticorps produits ex vivo, dirigés contre l’α-synucléine anormale ou des fragments de cette dernière
Source : Revue Neurologies
